| Imunitní reakce na nádory a protinádorová vakcinace |
|
prof. MUDr. Jiřina Bartůňková DrSc. |
| SANQUIS č.82/2010, str. 68 |
| Vznik nádorového onemocnění je mnohastupňový proces komplexní povahy, v němž samotné nádorové buňky představují velmi heterogenní populaci, zasazenou do kontextu mikroprostředí nenádorových buněk a tkání, jež tvoří složitý nádorový „ekosystém“.
|
|
Imunitní systém je schopen kontrolovat růst nádorových buněk v raných stadiích vzniku nádoru. S pokročilým růstem nádoru se imunitní mechanismy víceméně paralyzují a mnohdy mají naopak podpůrný účinek ve prospěch proliferace nádorových buněk. Aby byla protinádorová terapie úspěšná, musí zohledňovat všechny komplexní aspekty interakce imunitního systému a nádorových buněk včetně mikroprostředí. Článek se zaměřuje na problematiku nádorových vakcín založených na dendritických buňkách, které jsou použitelné u již diagnostikovaných nádorových onemocnění u lidí jako léčebná vakcinace spolu s dalšími léčebnými modalitami.
|
|
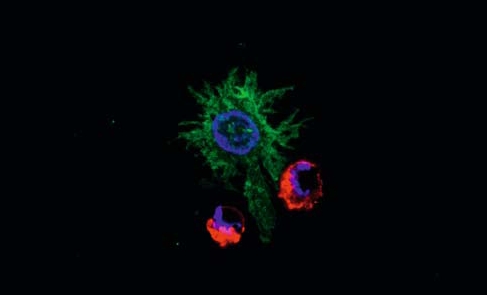 | | Dendritické buňky mají zásadní roli v protinádorové imunitní reakci |
|
|
Důkazy pro roli imunitního systému v kontrole nádorového růstu
Vznik nádorového onemocnění je mnohastupňový proces komplexní povahy, v němž samotné nádorové buňky představují velmi heterogenní populaci navíc zasazenou do kontextu mikroprostředí nenádorových buněk a tkání (cévy, stromální buňky, mezibuněčná hmota, infiltrující buňky imunitního systému aj.), tvořící složitý nádorový „ekosystém“ (obr. 1). Existují důkazy pro to, že imunitní systém je schopen kontrolovat růst nádorových buněk v raných stadiích karcinogeneze i ve stadiu tzv. preneoplázie. S pokročilým růstem nádoru se imunitní mechanismy víceméně paralyzují a mnohdy mají naopak podpůrný účinek ve prospěch proliferace nádorových buněk, za což jsou zodpovědné různé únikové mechanismy nádorových buněk.
V boji proti nádorovým buňkám používá imunitní systém obě hlavní složky – systém přirozené (nespecifické) imunity (makrofágy, NK buňky, granulocyty, komplement) i systém imunity adaptivní (specifické T a B lymfocyty). Spojkou mezi oběma systémy jsou buňky dendritické (DC), které reagují na signál „nebezpečí“ a imunitní reakci adekvátně podle druhu podnětu směrují. Imunitní reakce na nádorovou buňku se tedy v principu neliší od reakce například na buňky infikované viry. Hlavním problémem je však rozpoznání nádorové buňky jako cizorodého elementu a vydání adekvátního signálu „nebezpečí“, který by spustil celou kaskádu imunitních reakcí. Nádorová buňka vychází z vlastních buněk organismu, ke kterým je ustanovena tolerance. Principem imunoterapie je právě vybudit různými způsoby složky imunity tak, aby nádor „netolerovaly“, ale naopak vyvinuly proti němu účinnou imunitní reakci a překonaly různé únikové mechanismy nádorových buněk před imunitním systémem.
|
|
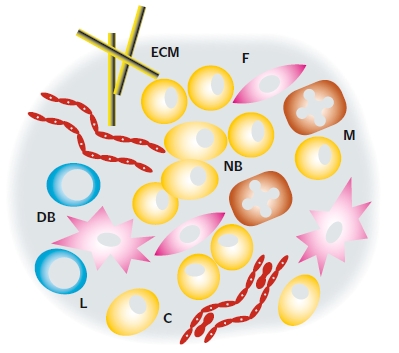 | | Obr. 1: Nádorový ekosystém
NB – nádorová buňka, ECM – extracelulární matrix, F – fibroblast,
M – makrofágy, DB – dendritická buňka, L – lymfocyty,
C – céva. Podle Klener P.: Nová protinádorová léčiva a léčebné
strategie v onkologii, Grada, Praha 2010. |
|
|
Editace nádoru imunitním systémem
Hypotéza nazývaná „Cancer immune editing“, tj. editace nádoru imunitním systémem, popisuje vztah nádoru a imunitního systému: ten vyvíjí na nádorové buňky neustálý tlak, který vede k selekci takových variant transformovaných buněk, jež dokáží uniknout efektorovým mechanismům imunitního systému. V procesu boje imunitního systému proti nádorovým buňkám existují tři úrovně – eliminace transformované buňky, ustanovení rovnováhy mezi transformovanou buňkou a organismem (equilibrium) a únik transformované buňky před kontrolou imunitního systému (escape).
Ve většině případů je nádorová buňka rozpoznána v časných stadiích transformace a zničena. Proces zde může skončit, nebo přejít do dalších fází. Ve fázi ustanovení rovnováhy hostitelský imunitní systém a přežívající nádorové buňky vcházejí do stadia dynamické rovnováhy. Nekonečná přizpůsobivost nádorových buněk vyplývající z rostoucí genetické nestability nakonec dá vzniknout novým genotypům, jež zmenší imunogenicitu, a může dojít k fázi úniku buňky před vlivem imunitního systému.
Fáze ustanovení rovnováhy je nejdelší z těchto tří procesů a klinicky se nejvíce shoduje s preneoplastickým onemocněním, které nejčastěji zůstává nediagnostikované. Výsledkem stadia rovnováhy mohou být tři různé situace: 1) kompletní eliminace nádorových buněk; 2) dlouhodobé, možná stálé udržení dynamické rovnováhy mezi aktivní imunitní odpovědí a vymezenou populací nádorových buněk; 3) únik před kontrolou imunitní reakce a rozvoj klinického onemocnění. Imunoterapie by měla přispět buď ke kompletní eliminaci, nebo spíše k dlouhodobému udržení rovnováhy.
Dendritické buňky jako centrální spojka mezi nespecifickou a specifickou imunitou
Pro ústřední úlohu dendritických buněk v účinné protinádorové imunitní reakci se nejvíce imunoterapeutických postupů zaměřuje právě na tyto buňky a na obnovení jejich adekvátní schopnosti rozpoznat a prezentovat nádorové antigeny. V posledních letech byla objasněna řada mechanismů, jež buňkám umožní rozeznat přítomnost mikroba či jiného nebezpečí včetně nádorových buněk v periferních tkáních a zajistí, že je zmíněná informace přenesena do lymfatických uzlin, kde jsou poté stimulovány specifické T-lymfocyty. Dendritické buňky (DC) byly pojmenovány podle charakteristické morfologie s množstvím výběžků, dendritů (obr. 2 na str. 69). V periferní krvi cirkulují dendritické buňky ve velmi malém množství, a proto se obtížně studují. Situace je navíc složitější, protože existuje celá řada subpopulací dendritických buněk s různými fenotypy i funkcemi. Pro imunoterapii se používají DC obvykle pěstované z monocytů periferní krve diferencované a maturované in vitro různými způsoby.
|
|
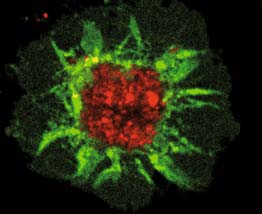 | | Obr. 2: Dendritická buňka s pohlcenými kousky nádorové
buňky (fotografie z konfokálního mikroskopu Olympus,
z publikace pracovníků Ústavu imunologie 2. LF UK a FNM
v Clinical Immunology, 2007) |
|
|
Využití dendritických buněk v imunoterapii nádorových onemocnění
Poznání klíčové role dendritických buněk v procesu zahájení imunitní reakce a možnost jejich přípravy ve velkém množství in vitro vedly k úvahám o jejich využití v imunoterapii nádorových onemocnění. Je třeba poznamenat, že imunoterapie nádorů se neomezuje jen na dendritické buňky, ale jsou studovány nejrůznější přístupy s využitím složek jak nespecifické imunity, tak specifické. Zde jsou zmíněny jen vakcíny na bázi dendritických buněk.
Obecné schéma imunoterapie dendritickými buňkami je znázorněno na obrázku 3. Monocyty periferní krve pacientů vybraných pro imunoterapii se získávají v průběhu leukaferézy. Z monocytů se pak připraví v laboratoři dendritické buňky. V dalším kroku se DC „pulzují“ nádorovými antigeny. Po pohlcení nádorových buněk jsou následně dendritické buňky aktivovány a jsou poté jako protinádorová vakcína podány zpět pacientovi. Různé výzkumné skupiny nebo biotechnologické firmy se ve výrobním postupu liší a obvykle jsou tyto postupy patentově chráněny.
Rychle po objasnění role dendritických buněk v indukci imunitní reakce a publikaci protokolů pro jejich přípravu z monocytů bylo provedeno v posledních 10 letech několik stovek klinických studií u řady nádorových onemocnění (např. maligní melanom, renální karcinom, non-Hodgkinský lymfom, glioblastom, karcinom prostaty a další). U většiny těchto studií došlo k laboratorně detekovatelné indukci protinádorové imunitní odpovědi, ale i přes několik popsaných regresí nádorových lezí nebyl klinický efekt většinou dlouhodobý.
Zásadním problémem provedených studií je, že do nich byli zahrnuti výlučně pacienti ve velmi pokročilých fázích onemocnění, u kterých byly již vyčerpány všechny ostatní terapeutické modality. Imunitní systém byl tedy výrazně poškozen jak proběhlou chemoterapií, tak imunosupresivními mechanismy nádorové tkáně. Není překvapující, že za takových podmínek je naděje na trvalý efekt imunoterapie malá. Je spíše překvapující a povzbudivé, že většinou došlo k indukci detekovatelné imunitní odpovědi a ojedinělým výrazným klinickým efektům.
|
|
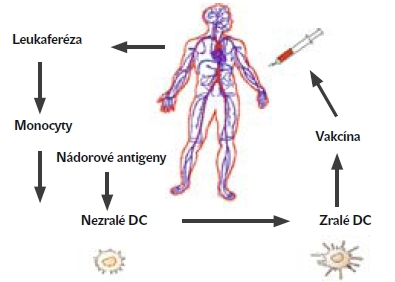 | | Obr. 3: Obecné schéma protinádorové imunoterapie pomocí
vakcíny z dendritických buněk |
|
|
Nové poznatky o účinku chemoterapeutik také vedly ke konceptu kombinované chemo-imunoterapie. Některá chemoterapeutika totiž indukují tzv. imunogenní smrt buňky. Předpokládá se, že vhodné načasování chemoterapie a imunoterapie může zvrátit fázi úniku nádorových buněk do fáze equilibria podle výše zmíněné hypotézy a zajistit úspěch imunoterapie i u pacientů s pokročilejšími stadii onemocnění. Důkaz o účinnosti tohoto postupu přinesla vakcína z dendritických buněk Provenge americké firmy Dendreon. Fáze III. klinické studie prokázaly, že aplikace této vakcíny u pacientů s hormon-refrakterním karcinomem prostaty v kombinaci s chemoterapií statisticky významně prodloužila celkové přežití ve srovnání se skupinou bez vakcíny (o cca 4,5 měsíce, což je srovnatelná doba např. s chemoterapeutikem docetaxelem a jde o obvyklý výsledek v rámci testování nových protinádorových léčiv).
Na základě výsledků těchto několikaletých studií letos v dubnu schválila americká FDA tento preparát ke klinickému použití a zařadila jej do léčebných postupů u této kategorie nemocných. Jde vůbec o první protinádorovou individuální buněčnou vakcínu schválenou k rutinnímu klinickému použití.
V souladu s teoretickými předpoklady i experimentálními daty má protinádorová imunoterapie největší šanci na úspěch v případě, že bude aplikována pacientům v časných fázích onemocnění, případně pacientům po radikálním chirurgickém výkonu. Také se mezitím objasnily některé další mechanismy imunitní reakce, které mohou celkový výsledek vakcinace ovlivnit. V dalších studiích bude třeba brát v úvahu ev. manipulaci imunitního systému příjemce za účelem omezení inhibičních mechanismů imunity, např. cílením na T regulační buňky, ev. zohlednit individuální imunitní reaktivitu pacienta a kombinovat léčbu s jinými přístupy ve smyslu moderní koncepce „personalised medicine“. Imunoterapie tak může obohatit mozaiku komplexní terapie nádorových onemocnění, která zahrnuje různé léčebné modality zaměřené na jednotlivé složky ekosystému nádoru (obr. 4).
|
|
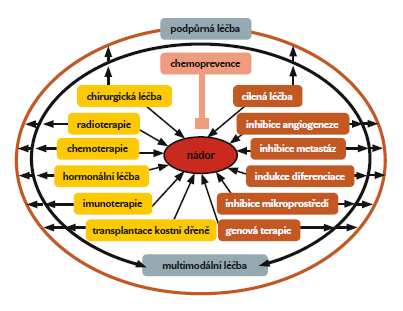 | | Obr. 4: Imunoterapie jako součást komplexní protinádorové
terapie. Podle Klener P.: Nová protinádorová léčiva a léčebné
strategie v onkologii, Grada, Praha 2010. |
|
|
Výzkum protinádorových vakcín v Ústavu imunologie 2. LF UK a FN Motol
Na Ústavu imunologie 2. LF UK a FNM je v posledních deseti letech vyvíjena a testována vakcína na bázi dendritických buněk proti karcinomu prostaty a ovaria. Výrobní postup se snažil zohlednit nejnovější poznatky základního výzkumu. Přesto zůstává mnoho neobjasněných otázek, které mohou zodpovědět až plánované klinické studie. Jde především o množství podávaných dendritických buněk v jedné aplikaci, způsob podání, frekvenci a celkovou dobu podávání protinádorové vakcíny. Neméně důležitým problémem je také typ testů, které budou používány pro monitoraci efektu terapie, což není dosud na celosvětové úrovni vyřešeno.
Kromě principiálních problémů kolem vakcinace dendritickými buňkami je zapotřebí brát v úvahu platnou legislativu. Imunoterapie dendritickými buňkami patří do metod moderní buněčné terapie a tento postup spadá podle evropské legislativy od roku 2003 pod zákon o léčivu. Znamená to, že veškerá manipulace s buňkami při přípravě vakcíny se musí odehrávat v superčistých prostorách za podmínek správné výrobní praxe (GMP) s povolením národních regulačních autorit (v České republice je to Státní ústav pro kontrolu léčiv). Registraci léčivého přípravku pak schvaluje Evropská léková agentura (EMA) na základě realizovaných adekvátních klinických zkoušek.
Ve FN Motol byla vybudována testovací superčistá laboratoř a po splnění náročných podmínek získala nemocnice Certifikát pro výrobu podle GMP od Státního ústavu pro kontrolu léčiv (SÚKL), čímž splnila legislativní předpoklady pro výrobu individuální vakcíny. V letošním roce byly zahájeny klinické studie fáze I/II schválené SÚKLem a registrované u Evropské lékové agentury, které mají prokázat bezpečnost přípravku a schopnost indukce imunitní reakce na nádorové struktury u definovaných skupin pacientů, jimž je tato vakcína podávána. Teprve výsledky ev. budoucí klinické studie fáze III. u stovek pacientů s nádory prostaty a pacientek s nádory vaječníku mohou přinést za několik let statisticky významné důkazy o případné účinnosti, na jejímž základě by se tato vakcína mohla zařadit do komplexní léčby příslušných nádorových onemocnění.
Finanční podpora: Projekt protinádorových vakcín na Ústavu imunologie 2. LF UK a FN Motol je podporován Výzkumným záměrem Ministerstva školství MSM 0021620812, grantem IGA MZ ČR NT1159: Téma grantu: „Fáze I/II klinické studie imunoterapie karcinomu prostaty pomocí vakcinace dendritickými buňkami.“, řešitel: Prof. MUDr. J. Bartůňková, DrSc., řešení projektu od 2010–2014, a grantem GA ČR 310/08/0838, téma grantu: „Příprava vakcín založených na dendritických buňkách pro protinádorovou imunoterapii karcinomu ovaria.“, řešitel: Doc. MUDr. Radek Špíšek, Ph.D., řešení projektu od 2008 do 2010, provozními prostředky FN Motol a sponzorskými dary.
Foto a schemata: archiv autorky
Celý článek ve formátu pdf naleznete zde.
|
|
|
 |
obsah čísla 82 |
 |
ročník 2010 |
 |
témata |
|

| SANQUIS PLUS |

|
| GALERIE SANQUIS |

|
| PORADNA |

|
|



